A calculadora de razão molar da Omni ajudará você a determinar a razão molar entre os diferentes reagentes e os diferentes produtos químicos de uma reação. Ela também pode ajudar determinar a massa ou o número de mols de cada composto químico exigido para performar a reação. Com esse conhecimento, você pode encontrar o agente limitante na reação ou qual composto químico está disponível em excesso.
Você está se perguntando o que é uma razão molar e como calculá-la? Quer saber a importância de uma razão molar? Junte-se a nós neste artigo para discutirmos a definição de uma razão molar, como determiná-la usando a fórmula da razão molar e como usá-la para obter mais informações de sua equação química balanceada.
A razão molar é diferente da fração molar. Nossa calculadora de fração molar 🇺🇸 é para onde você deve ir se tiver interesse na fração molar da sua solução.
O que é uma razão molar? Qual é a fórmula da razão molar?
A razão molar é a relação entre o número de mols (ou moléculas) de reagentes consumidos e o número de mols de produtos gerados em uma reação química. Você também pode expressá-la como a razão do número de mols de um reagente exigido para reagir completamente com outro reagente ou um produto produzido para outro produto.
Por exemplo, durante a produção de amônia, se 30 mols de hidrogênio reagem completamente com 10 mols de nitrogênio para dar 20 mols de amônia, então você pode escrever a razão molar entre os diferentes participantes da reação como:
Se você quiser encontrar a quantidade de cada elemento presente em um composto, a calculadora de composição centesimal 🇺🇸 da Omni pode te ajudar.
Como calcular a razão molar?
Para determinar a razão molar entre quaisquer dois elementos ou compostos em uma reação química:
- Faça o equilíbrio da reação química.
- Obtenha os coeficientes dos elementos ou compostos químicos correspondentes na equação balanceada.
- Calcule a razão entre esses coeficientes.
Em outras palavras, a fórmula para a razão molar entre quaisquer dois elementos ou compostos químicos é tão simples quanto:
onde:
- : qualquer elemento ou composto químico que reaja ou seja produzido na reação;
- : qualquer outro elemento ou composto químico que reaja ou seja produzido na reação;
- : coeficiente de na reação química equilibrada; e
- : coeficiente de na reação química balanceada.
O coeficiente em uma reação balanceada é útil para determinar a razão molar porque o coeficiente representa o número de moléculas desse elemento (ou composto químico) necessárias para que a reação ocorra sem deixar para trás qualquer excesso de reagentes.
Por exemplo, considere a seguinte equação química balanceada:
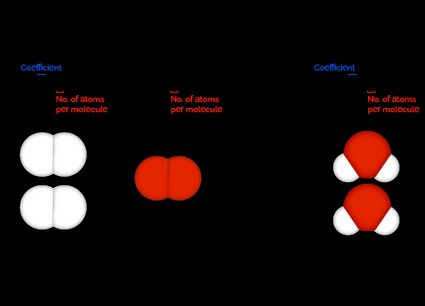
Com base nos coeficientes dessa reação química equilibrada, podemos obter as seguintes informações:
- Para cada duas moléculas de , é necessária uma molécula de para reagir completamente;
- Para cada duas moléculas de que reagem, duas moléculas de são formadas; e
- Para cada molécula de que reage, são formadas duas moléculas de .
Esse resultado também significa que, se tivéssemos vinte moléculas de hidrogênio, precisaríamos de dez moléculas de oxigênio para reagir completamente com ele e produzir vinte moléculas de água.
Em todo equilíbrio de reação, essa proporção entre o número de moléculas se mantém entre os diferentes reagentes e produtos. Um mol de uma substância é simplesmente a agregação de de átomos ou moléculas. Use nossa calculadora do número de avogadro para entender isso melhor.
O significado de uma razão molar e sua equação
Agora que você sabe como determinar a razão molar de uma reação química, vamos aprender sua importância.
Uma vez que você tenha a razão molar, poderá configurar quantos mols de cada item são necessários para a reação acontecer completamente. Por exemplo, se a razão molar entre dois reagentes for 2:3 e você tiver do primeiro reagente, então o número de mols do segundo reagente exigido é dado por:
Você pode usar a razão molar e o peso molecular das moléculas para determinar a massa dos elementos (ou compostos químicos) exigidos para completar a reação. Use a nossa calculadora de gramas para mols e a nossa calculadora de mols para entender como o peso molecular e a massa molar de um composto estão relacionados e como converter o número de mols para a massa do composto exigido. Portanto, depois de saber como encontrar a razão molar e numerar os mols exigidos, você pode “converter” a razão molar em gramas ou razão de “massa”:
Como a razão molar ajuda a determinar quanto de cada substância é exigida para completar a reação, você também pode usá-la para descobrir qual substância é o reagente limitante e qual substância está em excesso. Por exemplo, vimos que a equação da razão molar entre o hidrogênio e o oxigênio na produção de água é de 2:1. Se tivermos 12 mol de hidrogênio para 10 mol de oxigênio, saberemos imediatamente que o hidrogênio é o reagente limitante porque a reação exige que tenhamos 20 mol de hidrogênio. Também podemos dizer que o oxigênio está em excesso de 4 mol, pois somente 6 mol pode reagir com 12 mol de hidrogênio.
Como encontrar a razão molar usando esta calculadora de razão molar?
Essa calculadora de razão molar pode lidar com até cinco reagentes e cinco produtos. Além disso, há três tipos de cálculos que você pode escolher, explicados abaixo. Lembre-se de que, em todos esses casos, a razão molar resultante é exibida como uma tabela na parte inferior da calculadora.
-
O cálculo da razão molar a partir de uma reação equilibrada é o método mais simples. Nesta calculadora de razão molar, primeiro defina o
tipo de cálculocomocalcular razão molar. Em seguida, insira cuidadosamente os coeficientes de cada reagente e produto no campocoeficientecorrespondente. Você obterá a razão molar resultante na parte inferior como uma tabela. -
Quando tiver a razão molar, você poderá determinar o número de mols de cada reagente e produto exigido para completar a reação. Por outro lado, se você souber o número de mols necessários, poderá computar a razão molar. Nesta calculadora, primeiro defina
tipo de cálculocomocalcular razão molar e molse insira cuidadosamente os coeficientes ou o número de mols nos campos correspondentes. Você obterá a razão molar resultante na parte inferior como uma tabela. -
É possível calcular a massa de cada reagente e produto exigido se você souber a razão molar, o número de mols exigido e o peso molecular de cada reagente e produto. Nesta calculadora, primeiro defina
tipo de cálculocomocalcular razão molar, mols e massa. Em seguida, insira os coeficientes, o número de mols e a massa nos campos correspondentes. -
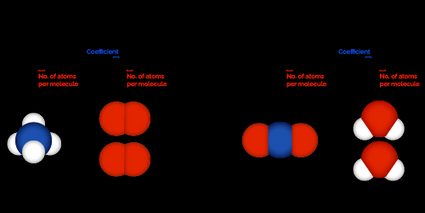
Para avaliar o peso molecular, precisamos conhecer cada elemento do composto químico, juntamente com o número de átomos por molécula. Por exemplo, para , digite no primeiro campo de
átomos por moléculase selecione como sua unidade. Em seguida, digite no segundo campo deátomos por moléculase selecione como sua unidade. Esta calculadora pode suportar até cinco elementos por reagente ou produto. -
Recomendamos que você utilize o campo
átomos por moléculaspara calcular o peso molecular, mas você pode inserir à mão qualquer valor no campo de peso molecular. A calculadora pode vir a mostrar a seguinte mensagem: “O número de átomos por moléculas deve ser um número inteiro positivo” Isso ocorre porque essa calculadora usa massas atômicas conforme listadas nos , e os valores que você está usando podem ser ligeiramente diferentes.
Perguntas frequentes
Como calcular a razão molar a partir do peso molecular?
Para determinar a razão molar a partir do peso molecular, você precisa da massa de cada substância.
- Se você converter o peso molecular da primeira substância em massa molar, você precisará da massa de cada substância.
- Divida a massa da primeira substância por sua massa molar para obter o número de mols usados (ou produzidos) na reação.
- Repita as etapas um e dois para a segunda substância para obter o número de mols usados (ou produzidos) na reação.
- Calcule a razão entre o número de mols das duas substâncias para obter sua razão molar.
Qual é a razão molar entre o sódio e o cloro na formação do sal de cozinha?
2:1. Para cada dois mols de sódio, é exigido um mol de cloro para formar dois mols de cloreto de sódio, comumente conhecido como sal de cozinha.
Como converter a razão molar em razão volumétrica?
A razão molar e a razão volumétrica são iguais se todos os gases que reagem e são produzidos estiverem na mesma temperatura e pressão.
- Calcule a razão entre o volume de um mol do primeiro gás e o volume de um mol do segundo gás em suas respectivas temperaturas e pressão.
- Multiplique essa razão pela razão molar para obter a razão de volume.
- Pronto, se orgulhe de ter resolvido esse problema complexo.
Como calcular a razão molar a partir da massa?
Para calcular a razão molar a partir da massa dos reagentes (ou produtos), siga os passos abaixo:
- Calcule a massa molar de cada substância avaliando seu peso molecular.
- Divida a massa da primeira substância por sua massa molar para obter o número de mols usados (ou produzidos) na reação.
- Repita o passo a passo para a segunda substância para obter o número de mols usados (ou produzidos) na reação.
- Calcule a razão entre o número de mols das duas substâncias para obter sua razão molar.